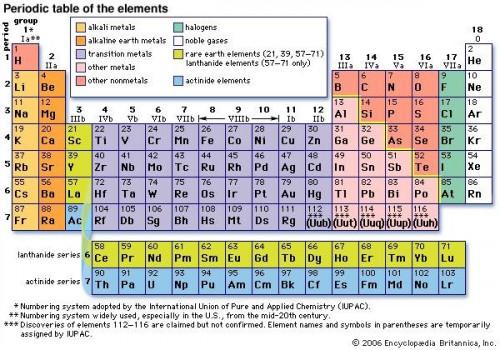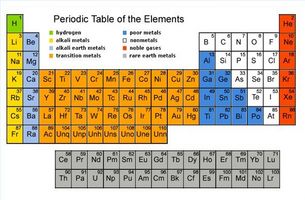
Le tableau périodique est un tableau scientifique qui organise les métaux connus dans un format facile à lire. Le tableau périodique est la pierre angulaire de la chimie et de notre compréhension de la façon dont les éléments réagissent les uns aux autres dans la nature. Le premier tableau périodique des métaux a été conçu par Dmitri Mendeleev en 1869 et contenait 65 des métaux connus. Le tableau périodique des métaux contient maintenant 117 éléments ou des métaux. Dmitri Mendeleev des éléments disposés en poids atomique avec le métal lourd vers la gauche et les éléments ayant des propriétés chimiques similaires dans la même colonne. Le tableau périodique des métaux combine également les métaux dans des groupes similaires. Ces groupes sont les métaux alcalins, les métaux alcalino-terreux, les halogènes, les gaz rares, les métaux de transition, des métaux des terres rares, d'autres métaux et d'autres métaux non-terreux.
Instructions
Commencez par regarder le tableau. Les lignes sont appelées périodes et sont énumérés dans l'ordre de leur numéro atomique du plus bas au plus élevé. Le numéro atomique représente le nombre de protons présents dans le noyau de leurs atomes. Les colonnes sont appelés groupes. Les groupes sont considérés comme les moyens les plus importants de l'identification des métaux. Les groupes sont appelés métaux alcalins, les métaux alcalino-terreux, les halogènes, les gaz rares, les métaux de transition, des métaux des terres rares, d'autres métaux et d'autres métaux non-terreux. Les groupes indiquent des propriétés chimiques semblables et le même type de configurations d'électrons dans leur couche de valence.
Les électrons dans l'enveloppe extérieure sont appelés valence électrons, qui déterminent la façon réactive un métal est à d'autres métaux. Les chiffres romains au-dessus de chaque groupe d'éléments spécifient le nombre habituel d'électrons de valence. «A» et «b» inclus à côté des chiffres romains pour déterminer où se trouvent les électrons. éléments représentatifs sont «a» et leurs électrons résident dans le "s" et "p" sous-niveaux. Les éléments non représentatifs sont «b» et leurs électrons se trouvent dans le "d" et "f" sous-niveaux.
2 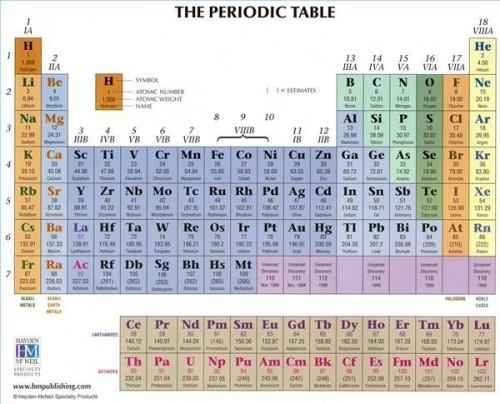
Regardez le tableau et le fer, ou Fe. Fe signifie le mot latin ferrum. Fe possède une série de nombres qui l'entourent. Pour localiser le fer trouvent dans le groupe 8 VIIIb. Au-dessus de l'abréviation de Fe est son numéro atomique, qui est 26. Habituellement en dessous du Fe est le poids atomique, qui est 55,847. Certains tableaux périodiques varient dans une certaine mesure dans l'information et de la configuration, mais le numéro atomique et le poids atomique seront présents.
3 Remarquez un groupe distinct des métaux au fond. Ce groupe est appelé les métaux des terres rares. La plupart des métaux des terres rares sont artificielle. Il y a 30 de ces métaux, et ils résident dans le groupe 3 en lignes 6 et 7. Ces métaux comprennent deux séries de métaux appelés lanthanides et des actinides.