En chimie, une taupe est une quantité utilisée se rapportent à des produits réactifs dans les équations stoechiométriques. Une mole de toute substance est égale à 6,02 x 10 ^ 23 particules - habituellement des atomes ou des molécules - de cette substance. Pour un élément donné, la masse (en grammes) d'une mole est donnée par son nombre de masse sur le tableau périodique; la «masse moléculaire» d'une molécule est la somme des masses molaires des éléments dans la molécule dans les proportions correctes. Il est simple de déterminer la masse molaire des éléments et des molécules à l'aide du tableau périodique, ainsi que la conversion entre les grammes et les taupes.
Instructions
La détermination de la masse molaire d'un élément
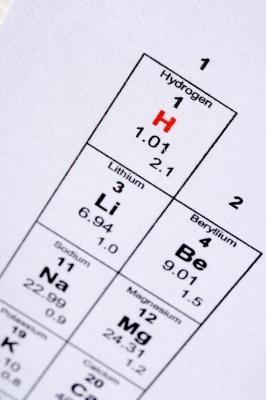
Trouver le lithium élément (Li) sur la table périodique. Le numéro atomique du lithium est égal à 3, représentant le nombre de protons dans le noyau d'un atome.
2 A noter que le nombre de masse de lithium est de 6,94, ce qui représente la somme des nombres de protons et de neutrons dans le noyau d'un atome.
3 A noter que le nombre de masse est égale à la masse (en grammes) d'une mole de lithium; ceci est la masse molaire du lithium.
Déterminer la masse moléculaire d'un composé chimique
4 Déterminer la masse moléculaire du dioxyde de carbone (formule chimique CO2). Trouver le carbone et l'oxygène dans le tableau périodique.
5 Noter que les masses de carbone et d'oxygène de la table périodique, qui sont 12,01 et 16, respectivement.
6 Ajouter les nombres de masse d'un atome de carbone et de deux atomes d'oxygène de la table périodique: 12.01 + 2 (16) = 44.01 grammes par mole
Conversion de masse à Moles
7 Calculer le nombre de moles d'eau dans 600 grammes d'eau (H2O). Trouver l'hydrogène et de l'oxygène dans le tableau périodique.
8 Mettre en place l'équation suivante relative grammes aux moles:
x moles H2O = (1 mole H2O / 18 grammes H2O) x (600 grammes H2O)
9 Résoudre l'équation à l'étape 2 pour trouver qu'il ya 3,33 moles de H2O dans 600 grammes de H2O.